Солі нітратної кислоти називають нітратами. Нітрати лужних металів, кальцію і амонію ще називають селітрами, наприклад: KNO3 – калієва селітра; NaNO3 – натрієва (чилійська) селітра; Ca(NO3)2 – кальцієва (норвезька) селітра; NH4NO3 – аміачна селітра.
Речовини, які містять необхідні для рослин елементи живлення, називаються мінеральними добривами.
Добрива вносять у ґрунт з метою одержання високих і стійких урожаїв. Найважливішими елементами для рослин є N, P і К. Без Нітрогену не можуть утворюватися білкові молекули, без Фосфору – нуклеїнові кислоти, вітаміни. Завдяки Калію прискорюється фотосинтез, зміцнюються стебла злакових рослин, покращується накопичення сахарози в цукрових буряках і крохмалю в картоплі.
Формула карбонатної (вугільної) кислоти – Н2СО3.
Солетворний оксид СО2 розчиняючись у воді утворює слабку кислоту, яка існує лише в момент її утворення. Кислота не стійка і відразу розкладається на вуглекислий газ і воду:
Н2СО3 ⇄ СО2↑+ Н2О.
Як двохосновна, вона дисоціює ступінчасто. Спочатку Н2СО3 ⇄ Н+ + НСО3–, а дальше у невеликій кількості НСО3– ⇄ Н+ + СО32–.
Усне повторення
1. Яку електронну структуру зовнішньої оболонки мають атоми елементів: Оксигену, Сульфуру, Нітрогену й Фосфору?
2. Що таке алотропні модифікації? Які алотропні модифікації характерні для Оксигену, Сульфуру й Фосфору?
Положення металічних елементів у періодичній системі
 Вам уже відомо, що більшість хімічних елементів являються металічними. Ці елементи є в усіх групах періодичної системи. Перші три групи складаються тільки з металічних елементів, за винятком Гідрогену в першій групі та Бору в третій групі. У IV, V, VI групах металічні елементи в побічних підгрупах і унизу головних підгруп. Якщо в періодичній системі елементів Д. І. Менделєєва провести умовну діагональ від Берилію до Астату, то в головних підгрупах зліва від діагоналі, у побічних підгрупах та у восьмій групі (виключаючи інертні гази) – металічні елементи. До металічних елементів належать також лантаноїди і актиноїди.
Вам уже відомо, що більшість хімічних елементів являються металічними. Ці елементи є в усіх групах періодичної системи. Перші три групи складаються тільки з металічних елементів, за винятком Гідрогену в першій групі та Бору в третій групі. У IV, V, VI групах металічні елементи в побічних підгрупах і унизу головних підгруп. Якщо в періодичній системі елементів Д. І. Менделєєва провести умовну діагональ від Берилію до Астату, то в головних підгрупах зліва від діагоналі, у побічних підгрупах та у восьмій групі (виключаючи інертні гази) – металічні елементи. До металічних елементів належать також лантаноїди і актиноїди.
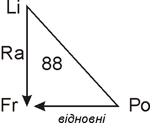
Атоми металічних елементів порівняно легко віддають валентні електрони і перетворюються на позитивно заряджені йони. Метали як відновники вступають в реакцію з різними окисниками, серед яких можуть бути прості речовини (H2, S, N2, Cl2, O2), складні речовини: кислоти, солі, вода. Найенергійніше метали реагують з галогенами, киснем, сіркою. Хімічні властивості металів можна зобразити за допомогою такої схеми:
Вироби з металів та їхніх сплавів, крім золота і платини, під впливом повітря, вологи поступово руйнуються в результаті хімічних реакцій, які самочинно відбуваються між металами і речовинами, що містяться в навколишньому середовищі. У результаті корозії змінюється зовнішній вигляд металу: гладенька, добре відполірована поверхня стає шорсткою, покривається різними продуктами корозії, якість виробів і споруд погіршується. Вони можуть стати навіть зовсім непридатними для використання. У результаті корозії залізні вироби покриваються бурим нальотом, вироби із цинку і алюмінію набувають білого чи сірого кольору. На поверхні мідних виробів появляється зеленкувато-блакитний наліт – це основна сіль (CuOH)2CO3, що є отруйною речовиною. Срібні предмети темніють.
Прості речовини елементів І групи головної підгрупи називаються лужними металами. Лужними вони називаються тому, що їх гідроксиди є сильними лугами. До цих елементів належать Літій, Натрій, Калій, Рубідій, Цезій і Францій.
Елементи другої групи головної підгрупи періодичної системи елементів Кальцій, Стронцій і Барій називають лужноземельними металами тому, що гідроксиди цих металів проявляють лужні властивості, а оксиди цих металів тугоплавкі і подібні до оксидів алюмінію і важких металів, які назвали землями. Пластичні метали, але значно твердіші за лужні метали, менш легкоплавні.
Зміст – 10 клас
- Тема 1. Неметалічні елементи та їхні сполуки
- §1. Загальна характеристика неметалічних елементів
- §2. Алотропні модифікації
- §3. Поширення неметалічних елементів у природі. Застосування неметалів
- §4. Хімічні властивості неметалів
- §5. Сполуки неметалічних елементів з Гідрогеном
- §6. Добування амоніаку. Солі амонію
- §7. Оксиди та гідратні форми оксидів неметалічних елементів
- §8. Сульфатна кислота
- §9. Сульфати. Застосування сульфатної кислоти та сульфатів
- §10. Нітратна кислота
- §11. Нітрати
- §12. Загальні відомості про азотні та фосфорні добрива
- §13. Карбонатна кислота і карбонати
- §14. Будівельні матеріали
- §15. Узагальнення і систематизація знань
- Тема 2. Металічні елементи та їхні сполуки
- §16. Загальні відомості про металічні елементи та метали
- §17. Хімічні властивості металів
- §18. Корозія металів
- §19. Лужні метали
- §20. Лужноземельні метали. Кальцій і Магній
- §21. Поняття про твердість води
- §22. Алюміній та сполуки алюмінію
- §23. Залізо та сполуки Феруму
- §24. Металічні руди. Загальні способи добування металів
- §25. Метали і сплави в сучасній техніці
- §26. Розвиток металургії в Україні. Охорона навколишнього середовища
- Відповіді – 10 клас
- Узагальнення й систематизація знань з теми “Металічні елементи та їхні сполуки”





















Останні коментарі
JESSESJUXXX у: 4.7. Розрахунки за хімічними рівняннями
У першій задачі помилка, у заліза не 2 моль, а 1 моль, але кінцева відповідь вір ...
Наташа у: §21. Відношення об’ємів газів у хімічних реакціях
Пожалуйста срочно ответ на номер 249 и 525 в 21 параграфе ...
Ximiya у: §6. Масова частка розчиненої речовини
Дякуємо, виправили ...
Ximiya у: §24. Поняття про оксиди. Умови виникнення й припинення горіння
http://www.chemistry.in.ua/about ...
Ximiya у: §30. Метанол і етанол як представники насичених одноатомних спиртів
дякуємо, виправили ...