Людину оточує безліч речовин, деякі з них називають «чистими». Чиста речовина майже не містить домішок інших речовин. Так, у чистій воді містяться лише молекули води. Чиста мідь є речовиною, яка утворена лише атомами елемента Купруму.
Сучасна техніка потребує речовин, у яких масова частка сторонніх домішок не перевищує мільйонної частки. Такі речовини називають надчистими. Без них не могла б розвиватися радіоелектроніка. Але слід пам’ятати, що абсолютно чистих речовин у природі не існує, і добути їх штучно практично неможливо. Речовини завжди містять у своєму складі сторонні атоми чи молекули. Якщо їх маса значно менша за масу основної речовини, то вони називаються домішками. Якщо вміст домішок у речовині істотний, то утворюється суміш речовин.
Дуже малий вміст домішок часто не позначається на хімічних властивостях речовин, тому такі речовини називають хімічно чистими. Однак навіть мінімальні домішки нафтопродуктів роблять воду непридатною для пиття.
Суміші
Склад суміші може бути різний.
У житті, як правило, ми стикаємося із сумішами речовин. Суміш – це сукупність різних речовин, разом змішаних, але хімічно не з’єднаних. Речовини перемішуються, проте не реагують між собою і їх у принципі, можна розділити. Повітря, як ми знаємо – це суміш кількох речовин: кисню, азоту, вуглекислого газу тощо. Граніт, із якого роблять обеліски – це суміш кварцу, польового шпату і слюди. Нафта – це суміш понад ста речовин. Молоко також суміш. При його охолодженні і відстоюванні на поверхні спливає жир. Бензин теж суміш речовин.

Рис. 27. Суміш води з крейдою (зліва), чиста речовина – вода дистильована (справа).
Розрізняють суміші однорідні і неоднорідні.
Частинки компонентів рівномірно розміщені у суміші. Однорідними сумішами є, наприклад, водний розчин кухонної солі, розчин цукру у воді, повітря, більшість металічних сплавів, суміш газів.
Фізичні властивості однорідної суміші частково відрізняється від фізичних властивостей її складових. Наприклад, температура кипіння чистої води становить +100°С, а з домішками солі температура кипіння підвищується.
Неоднорідними сумішами є, наприклад, ґрунт, молоко, каламутна вода, більшість мінералів.
Речовини, які входять до складу неоднорідної суміші зберігають свої фізичні властивості. Це можна підтвердити таким дослідом. Відомо, що залізо притягується магнітом і тоне у воді, а порошок сірки, якщо збовтати з водою, спливає на поверхню, бо не змочується нею. Змішавши на листку паперу порошкоподібне залізо з порошком сірки, отримаємо сірувато-жовту суміш. Опустимо частинку цієї суміші у воду і розмішаємо. Сірка і залізо розділяться: крупинки сірки спливуть на поверхню води, а крупинки заліза – потонуть. Решту суміші накриємо аркушем паперу і наблизимо до неї магніт. Крупинки заліза притягнуться (через папір) до магніту, а сірка залишиться на папері.

Рис. 28. Дослід з розділенням суміші заліза і сірки: а) порошкоподібне залізо; б) порошкоподібна сірка; в) суміш заліза і сірки; г) розділення суміші при розчиненні у воді; ґ) розділення суміші дією магніту.
Методи розділення сумішей
За допомогою фізичних методів суміші можна розділити на складові частини. Розділення сумішей ще називають очищенням речовин. Вважають, що очищують ту речовину, заради якої здійснюють розділення. Її в суміші може бути незначна кількість. Наприклад, у золотоносному шарі пустої породи незрівнянно більше, ніж золота.
Розділення сумішей (за властивостями)
| Однорідні (частинок не видно) | Неоднорідні (частинки видно) | ||
 |
 |
 |
 |
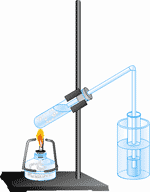
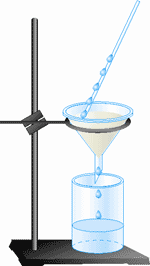
| перегонка | випаровування | фільтрування | відстоювання |
 |
 |
 |
|
| кристалізація | хроматографія | дія магнітом | |
Існує багато методів розділення сумішей. Щоб розділити суміш необхідно знати властивості речовин, які входять до її складу, тип суміші, агрегатний стан.
Таблиця 1.
Методи розділення сумішей
| Суміш |
Метод розділення |
Які суміші можна розділити |
Короткий опис |
| Однорідна | Перегонка або дистиляція | Суміші рідин з різними температурами кипіння | Суміш рідин повільно нагрівається. За цих умов речовина, яка має найнижчу температуру кипіння, випаровується раніше, її пари охолоджуються, конденсат збирається в окремій ємності. Приклад: добування дистильованої води, відокремлення спирту від води, розділення нафти на фракції |
| Випаровування | Розчинену тверду речовину з розчину | Суміш нагрівають. Рідина випаровується, а тверда речовина залишається у вигляді кристалів. Приклад: кухонну сіль з розчину солі | |
| Кристалізація | Розчинену тверду речовину із концентрованого розчину | Суміш твердої і рідкої речовини нагрівають. Після випаровування частини рідини, суміші охолоджують. Тверда речовина випаде в осад у вигляді кристалів. Приклад: кристалізація цукру у варені | |
| Хроматографія | Суміш розчинених речовин, які мають різну швидкість поглинання | У суміш опускають спеціальний хроматографічний папір. Компоненти суміші з різною швидкістю поглинаються цим папером. Кожен компонент зафарбовує папір у певний колір. Число кольорів вказує на число компонентів у суміші | |
| Неоднорідна | Фільтрування | Суміш розчинної і нерозчинної речовин, які мають різний розмір частинок | Суміш пропускають через фільтр. Нерозчинні речовини не проходять через пори фільтру і залишаються на ньому. Приклад: пісок, тирсу від розчину |
| Відстоювання | Суміш двох рідин, твердої нерозчинної речовини від розчину з різною густиною | Суміш відстоюють. Речовина, яка має більшу густину, осідає на дно, а яка має меншу густину – залишається на поверхні. Приклад: вода і олія, вода і тирса, вода і пісок | |
| Дія магнітом | Виділення твердої речовини, яка притягується магнітом | До суміші твердих речовин підносять магніт. Залізо притягується магнітом |
Людина широко використовує суміші у повсякденному житті. Наприклад, у будівництві використовують суміш цементу, піску, води. Для виробництва скла використовують суміш піску, соди, крейди. Лікарські речовини, які ви купуєте в аптеці, різні соки, чаї, компот – це теж суміші.
Підсумок
- Чиста речовина не містить домішок інших речовин.
- Суміш – це сукупність різних речовин, кожна з яких зберігає свої властивості.
![]()
- Суміш можна розділити на компоненти за допомогою механічних прийомів.
- Розділення сумішей – це виділення з неї чистих речовин.
- Яку речовину називають чистою?
- Що таке суміш?
- Які природні суміші ви знаєте?
- Які бувають суміші?
- Якими способами можна розділити неоднорідні суміші?
- Чим однорідна суміш відрізняється від неоднорідної?
Допитливим. Цифри і факти
Для дихання ми використовуємо повітря. Повітря – це суміш газів. Чи відомо вам, як змінюється склад вдихуваного і видихуваного повітря?
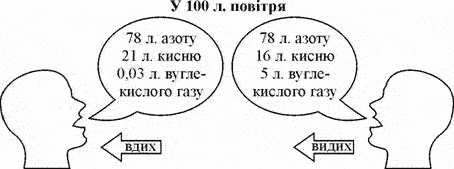
Рис.29. Склад вдихуваного і видихуваного повітря.
Вміст вуглекислого газу збільшується у 167 разів! Вуглекислий газ негативно впливає на самопочуття людей.
Домашній експеримент
Очищення срібних речей
 Візьміть на тарілочку 50 г крейди, добавте до неї 30 г 10% розчину нашатирного спирту (гідроксиду амонію), перемішайте скляною паличкою. Добутою сумішшю натріть срібний браслет (сережку, колечко), промийте його теплою водою, витріть насухо ватою.
Візьміть на тарілочку 50 г крейди, добавте до неї 30 г 10% розчину нашатирного спирту (гідроксиду амонію), перемішайте скляною паличкою. Добутою сумішшю натріть срібний браслет (сережку, колечко), промийте його теплою водою, витріть насухо ватою.



















2 коментарі
Валентина
домашня робота-напишіть послідовність очищення крейди зі сілью окремо на чистій речовині
Серафима
ОГО!Ничего себе!Больше информации чем в книге!!!!