Думку про те, що всі тіла складаються з найдрібніших, невидимих, неподільних частинок, які вічно рухаються – атомів, висловив давньогрецький філософ Демокріт 2500 років тому. Проте, довести це експериментально він не міг. Вчення про атоми й молекули розробив у середині XVIII столітті російський вчений Михайло Васильович Ломоносов.

М. В. Ломоносов
Він твердив, що тіла в природі складаються з корпускул (молекул), до складу яких входять елементи (атоми). Конкретніші уявлення про атоми виникли значно пізніше внаслідок розвитку фізики та хімії, що базувалися на науковому експерименті. Те, що атоми справді існують, було підтверджено експериментально. Так, під час пропускання постійного електричного струму крізь воду в апараті для розкладання води, в одній із трубок (1) приладу збирається газ, в якому тліюча скіпка яскраво спалахує. Це – кисень. В іншій трубці (2) удвічі більше газу, який займається від запаленої скіпки. Це – водень. Процес розкладання води можна описати так: найдрібніша частинка води (молекула води), яка утворена двома атомами Гідрогену й одним атомом Оксигену, під час пропускання постійного електричного струму розкладається на атоми. Потім однакові атоми з розкладених молекул з’єднуються по два.

Рис. 30. Апарат для розкладання води.
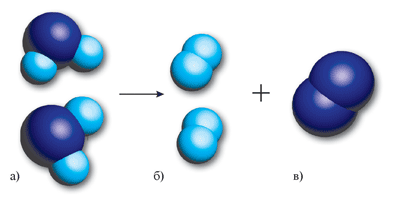
Рис. 31. Схема розкладу молекули води (а) та утворення молекул водню (б) та кисню (в).
Із двох молекул води утворюється одна двохатомна молекула кисню (з атомів Оксигену) і дві двохатомні молекули водню (із атомів Гідрогену).
З винайденням оптичних приладів, які дають дуже велике збільшення, вдалося спостерігати атоми.

Рис. 32. Атоми Ніколу та Платини.
Кожне тіло у всесвіті, навіть найвіддаленіша зоря складається з атомів. Окремі атоми надто маленькі, щоб їх можна було побачити, але з’єднавшись разом, вони утворюють усі відомі хімічні речовини. Деякі з цих речовин тверді, чи рідкі й видимі, інші ж газоподібні й невидимі. Найкрихітніша частинка, яку можна роздивитися у звичайний мікроскоп, складається з десяти мільярдів атомів.
Що ж являє собою атом? Яка його будова?
Атоми мають складну будову. Вони складаються із протонів, нейтронів і електронів. Кожна з цих частинок має певну масу. Маси протонів і нейтронів майже однакові (mp+ = 1,0073, mn0= 1,0086 в а.о.м.), а маса електрона у 1840 разів менша маси протона ( me–= 0,00055).
Кожний атом має ядро і електронну оболонку.
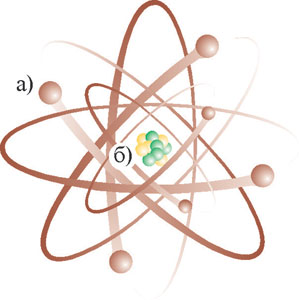
Рис. 33. Будова атома: а) електронний шар з електронами; б) ядро з протонами та нейтронами.
Атомне ядро – центральна частина атома, що складається із більших у порівнянні з електроном частинок протонів і нейтронів. У ядрі зосереджена основна маса атома. Елементарні частинки ядра утримуються так званими ядерними силами. Навколо ядра на значній віддалі від нього обертаються зовсім маленькі частинки – електрони, які утворюють негативно заряджену електронну оболонку атома.
Електрони утримуються біля ядра атома силами електричного притягання, оскільки мають протилежний протонам заряд.
Маса електрона дуже маленька, тому можна вважати, що вся маса атома сконцентрована у ядрі.

Рис. 34. Порівняння маси ядра й електрона.
Однак, радіус ядра атома в десятки разів менший за радіус атома з електронами, розміщеними в електронному шарі. Число протонів в атомі дорівнює числу електронів, тому атом в цілому електронейтральний. Число протонів збігається з порядковим номером елемента в періодичній таблиці елементів. Д. І. Менделєєва.
Наприклад, ядро атома Гідрогену складається лише з одного протона із зарядом +1 і одного електрона. Порядковий номер Гідрогену рівний одиниці.
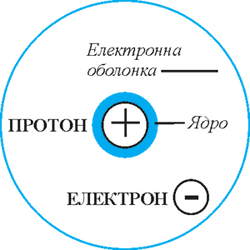
Рис. 35. Будова атома Гідрогену.
У атома Гелію два протони і два нейтрони у ядрі і два електрони навколо ядра.
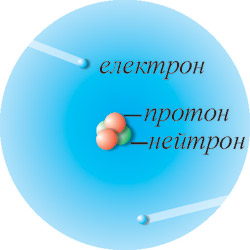
Рис. 36. Будова атома Гелію.
У перекладі з грецької мови слово «атом» означає «неподільний». Нині відомо, що й атоми можна поділити на ще дрібніші частинки.
Йони
Як нам уже відомо, атом є електронейтральний. Атом Гідрогену складається з ядра із зарядом +1 і електрона із зарядом –1. Та якщо із атома Гідрогену вилучити електрон, баланс зарядів порушиться, залишиться частинка, яка являє собою ядро атома із зарядом +1. Її позначають Н+ і називають йоном Гідрогену.
Атоми деяких хімічних елементів легко і охоче втрачають або набувають електрони, перетворюючись на зарядженні частинки. Атоми металічних елементів зазвичай легко втрачають від одного до трьох електронів, перетворюючись на позитивно заряджені йони, або катіони: Na+, K+, Mg2+, Ca2+, Cu2+, Al3+, Fe3+. Атоми неметалічних елементів, навпаки, краще приєднують до себе електрони, перетворюючись на негативно заряджені йони, або аніони: Cl–, O2–, S2–, N3–, C4–. Так, атому Літію вигідно віддати свій один електрон, а атому Флуору вигідно прийняти один електрон. При цьому атом Літію перетворюється на позитивно заряджений йон Li+, а атом Флуору – на негативно заряджений йон F–.
|
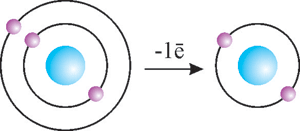
Атом Літію Li0 |
Йон Літію Li+ |
 |
|
|
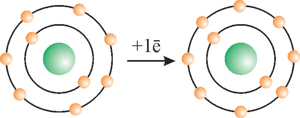
Атом Флуору F0 |
Флуорид-йон F– |
 |
|
Позитивний йон містить більше протонів ніж електронів.
Негативний йон містить більше електронів ніж протонів.
У перекладі з грецької слово «йон» означає «той що йде» – в електричному полі заряджені частинки на відміну від електронейтральних, здатні рухатися.
Отже, під час взаємодії між собою атоми можуть втрачати або приєднувати електрони і ставати зарядженими (позитивно або негативно). Різні атоми можуть віддавати або приєднувати річне число електронів.
Здатність атомом приєднувати або віддавати електрони залежить від заряду ядра, числа електронів в електронному шарі і розташуванням електронів навколо ядра.
Йони можуть існувати самостійно, однак їх властивості відрізняються від властивостей атомів. Атоми Гідрогену, приміром, утворюють двохатомні молекули водню, які існують у газоподібному стані, йони Гідрогену існують у розчинах і надають кислотам кислий смак. Атоми Хлору утворюють просту речовину Cl2 – отруйний газ жовто-зеленого кольору з різким запахом. Атоми Натрію сполучаючись між собою утворюють просту речовину – сріблясто-білий твердий метал з металічним блиском. Кухонна сіль NaCl утворена йонами Na+ і Cl–, безбарвна кристалічна речовина без запаху, неотруйна, немає металічного блиску.
Йони, як правило, утворюються в процесі розчинення речовин.
Молекули
Атоми можуть по-різному сполучатися один з одним. Як при складанні букв алфавіту утворюються сотні тисяч різних слів, так з атомів утворюються або молекули, або кристали різних речовин. До складу молекули можуть входити від двох однакових або різних атомів, а можуть декілька десятків, сотень і навіть тисяч.

Рис. 37. Схема молекули ДНК.
Молекула являє собою певну групу міцно зв’язаних атомів. Слово походить від латинського «moles», що означає «дуже маленька маса».
Із молекул побудовано багато речовин. Відомо, наприклад, кілька речовин утворених усього з двох видів атомів: атомів Оксигену і атомів Гідрогену. До таких речовин належать: водень, кисень, озон, вода.
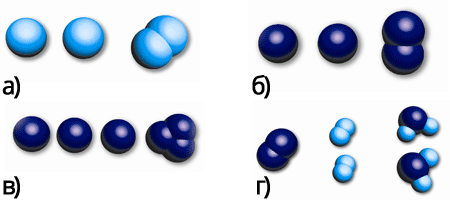
Рис. 38. Схема молекул: а) два атоми Гідрогену утворюють молекулу водню; б) два атоми Оксигену утворюють молекулу кисню; в) три атоми Оксигену утворюють молекулу озону; г)одна молекула водню і дві молекули кисню утворюють дві молекули води.
Два атоми Гідрогену, з’єднуючись між собою, утворюють молекулу водню. Два атоми Оксигену утворюють молекулу кисню, три атоми Оксигену – молекулу озону. Два атоми Гідрогену і один атом Оксигену утворюють молекулу води. У цій молекулі атом Оксигену зв’язаний з кожним із атомів Гідрогену.
Не можна говорити, що молекула зберігає всі властивості речовини, тому що фізичні властивості речовини – густина, твердість, температура плавлення та інші – зумовлюються сукупністю молекул даної речовини, характером її внутрішньої будови.
Чи можна сказати: «алмаз складається з атомів Карбону, що мають надзвичайну твердість»?
Подібно до молекул, атоми – структурні одиниці речовини характеризують її хімічний склад і хімічні властивості.
Підсумок
- Атоми складаються з електронів, протонів, нейтронів. Протони і нейтрони розміщені у ядрі атома, а електрони – в електронній оболонці.

- Молекула – електронейтральна частинка речовини, що складається з кількох атомів.
- Йон – це заряджений атом.
- Втрата атомом електронів перетворює його на позитивно заряджений йон.
- Приєднання атомом електронів перетворює його в негативно заряджений йон.
?
- Що таке атом?
- Що таке молекула?
- Що таке йон?
- З яких частинок складається атом?
- Чим протони відрізняються від електронів?
- Чому атом електронейтральний?
- Чому маса атома зосереджена в ядрі?
- У якому випадку атом перетворюється на йон?
Цифри і факти
• Якщо покласти впритул 200 мільярдів атомів Гідрогену, то утвориться «нитка» довжиною лише один метр.
• У одній краплинці води налічується сто квінтильйонів атомів. Число, що в нашій системі числення зображується одиницею із 20 нулями.
• Крихітна частинка пилу, ледь видима неозброєним оком, складається з квадрильйона (1015) атомів.
• Найлегший з атомів – атом Гідрогену, найважчий з існуючих у природі – атом Урану. Його маса у 238 раз перевищує масу атома Гідрогену.
• Екран комп’ютерного монітора і телевізора – це частина катодної трубки, на якій потік електронів малює світлове зображення.
Допитливим
У атома Гідрогену є один електрон, який обертається навколо ядра атома мільярди разів за мільйонну частку секунди і таким чином надає атому форму й змушує його поводитися так, ніби він суцільний. Аби зрозуміти, наскільки атом порожнистий, спробуйте уявити співвідношення між розміром ядра атома Гідрогену та відстанню до його електрона. Якби це ядро, що складається з одного протона, було завбільшки з тенісний м’ячик, то електрон обертався б навколо нього на відстані трьох кілометрів.
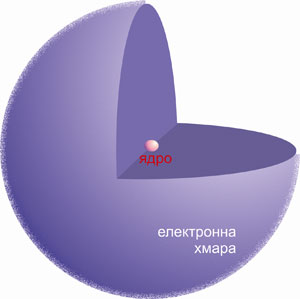
Рис. 38. Модель атома Гідрогену.
• Багато молекул мають специфічний запах. Так молекули гідроген сульфіду H2S, – утворюють газ, який має неприємний запах протухлих яєць. Достатньо замінити один єдиний атом Сульфуру на один атом Оксигену, щоб цей запах зник і утворилась нова речовина – вода.
Домашній експеримент
Атоми. Йони

На свіжий зріз картоплини крапніть розбавлений розчин йоду: з’явиться синій колір – це у присутності молекул йоду (J2) посинів крохмаль, який знаходиться у картоплі. На це ж місце на картоплині крапніть трішки розчину натрій сульфіту (Na2SO3), синє забарвлення швидко зникає.
Під дією натрій сульфіту йод перетвориться на заряджений йон J–, а в такому стані він уже не взаємодіє з крохмалем.



















1 коментар
Світлана
Яка Ви молодець! Дуже цікаво і корисно! Дякую.