Коли відомі хімічні формули всіх речовин, які вступили в реакцію, і тих, що утворилися в її результаті, хімічну реакцію можна виразити кількісним рівнянням.
Кожне рівняння реакції складається з двох частин. У лівій частині реакції записують формули реагентів, у правій – формули продуктів реакції. Обидві частини сполучають стрілкою (у схемі) або знаком «дорівнює» (у рівнянні реакції).
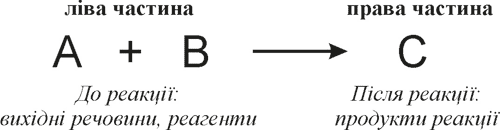
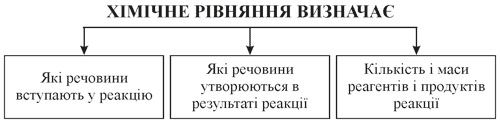
Схема 7. Хімічне рівняння
Приклад 1. Щоб скласти рівняння реакції горіння магнію, виконаємо дії у такій послідовності.
1. У лівій частині рівняння запишемо формули речовин, що вступили в реакцію і поставимо стрілку, а в правій частині запишемо формулу сполуки, що утворилася в результаті реакції. Формулу утвореної сполуки складаємо згідно валентності елементів.
Отримаємо схему реакції: ![]()
2. Згідно із законом збереження маси речовин ліва і права частини рівняння повинні мати однакову кількість атомів. Цього досягаємо, розставляючи коефіцієнти перед формулами речовин. Оскільки формули речовин складені згідно з валентністю, то змінювати індекси у формулах ми не маємо права. Починати можна урівнювати з того елемента, атомів якого більше.
До реакції число атомів Оксигену було два, а після реакції – один, тому перед MgO ставимо коефіцієнт «2». Число атомів Mg після реакції стало також 2, тому перед Mg у лівій частині рівняння ставимо коефіцієнт «2». Схема набуває вигляду: 2Mg + O2 → 2MgO.
Наведений запис називається схемою хімічної реакції.
3. Перевіряємо кількість атомів кожного елемента в лівій і правій частинах рівняння. Якщо їх числа співпадають,стрілку замінюємо на знак «дорівнює»: 2Mg + O2 = 2MgO.
Наведений запис називається рівнянням хімічної реакції.
Хімічне рівняння відрізняється від схеми реакції тим, що кількість атомів кожного елемента в лівій і правій його частинах однакова. Тому замість стрілки ставиться знак «дорівнює».
Приклад 2. Складемо хімічне рівняння реакції горіння фосфору.
1. Складаємо схему реакції: ![]()
Продукт реакції – фосфор(V) оксид. У лівій і правій частинах схеми – різна кількість атомів кожного елемента.
2. Добір коефіцієнтів починаємо з Оксигену. У лівій частині схеми є два атоми цього елемента, у правій – п’ять. Найменшим спільним кратним цих чисел є 10. Отже, у лівій і правій частинах схеми повинно бути по 10 атомів Оксигену. Знаходимо коефіцієнт для кисню. Поділимо 10 на 2, отримаємо п’ять (10 : 2 = 5). Отже, перед O2 ставимо коефіцієнт «5». Тепер знаходимо коефіцієнт для фосфор(V) оксиду. Діленням 10 на 5 отримаємо 2. Перед P2O5 ставимо коефіцієнт «2»: P + 5O2 → 2P2O5.
Тепер зрівняємо число атомів Фосфору. У правій частині є чотири атоми Фосфору (2 · 2 = 4), у лівій – один. Поставивши перед формулою фосфору коефіцієнт «4», отримаємо хімічне рівняння: 4P + 5O2 = 2P2O5.
З рівняння випливає, що з кожними чотирма атомами Фосфору взаємодіють п’ять молекул кисню і утворюються дві молекули фосфор(V) оксиду.
Правильно знайдені коефіцієнти мають бути найменшими з усіх можливих. Такі коефіцієнти не можна поділити без остачі на жодне однакове ціле число. Рівняння реакції складено правильно, якщо сума атомів кожного елемента до реакції дорівнює сумі атомів кожного елемента після реакції.
Приклад 3. Розглянемо реакцію взаємодії ферум(ІІ) хлориду з хлором: FeCl2 + Cl2 → FeCl3.
Якщо до реакції атоми одного і того ж елемента знаходяться у двох різних формулах, а після реакції в одній, то починаємо урівнювати з найменших індексів. До реакції число атомів Хлору – (2 + 2 = 4) чотири (парне число), а після реакції три (непарне число), спочатку подвоюємо непарне число атомів, тобто перед FeCl3 ставимо коефіцієнт «2» і урівнюємо число атомів Феруму зліва: 2FeCl2 + Cl2 = 2FeCl3.
Коефіцієнт перед формулою відноситься до всіх атомів даної речовини.
Приклад 4. У наведеному нижче рівнянні спочатку зрівнюємо число атомів Кальцію: 3CaO + P2O5 → Ca3(PO4)2
Якщо атоми одного елемента знаходяться в різних формулах, то їх кількість підсумовуємо:
До реакції вісім атомів Оксигену (3 + 5 = 8). Підраховуємо число атомів Оксигену після реакції. Індекс, що стоїть за дужками стосується всіх елементів в дужках, число атомів перемножуємо на індекс: 4 · 2 = 8 атомів Оксигену після реакції.
Приклад 5. У реакціях між складними речовинами можна урівнювати відразу цілими групами (кислотними залишками або гідроксигрупами): H3PO4 + Ca(OH)2 → Ca3(PO4)2 + H2O.
Груп атомів РО4 після реакції дві, а до реакції – одна, тому перед H3PO4 поставимо коефіцієнт два. Кальцію до реакції один атом, після реакції – три. Перед Ca(OH)2 поставимо коефіцієнт три. До реакції число атомів Гідрогену 12 (2∙3 + 3∙2), тому перед Н2О поставимо коефіцієнт шість: 2H3PO4 + 3Ca(OH)2 =Ca3(PO4)2 + 6H2O.
Отже, існують такі форми запису хімічної реакції:
- «Словесна» схема реакції: Магній + кисень = магній оксид.
- «Хімічна» схема реакції: Mg + O2 → MgO.
- Хімічне рівняння: 2Mg + O2 = 2MgO.
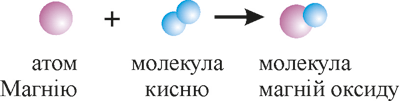
- Графічна – за допомогою моделей атомів і молекул.
Підсумок
Правила складання рівнянь хімічних реакцій:
- Потрібно знати формули речовин, що вступили в реакцію (формули реагентів), і формули речовин отриманих в результаті реакції (формули продуктів).
- Необхідно записати ліву частину рівняння, де розміщуються формули реагентів (у будь-якому порядку). Між формулами ставлять знаки плюс (+).
- Далі треба поставити стрілку і записати праву частину рівняння: формули продуктів (у будь-якому порядку) і знаки «плюс» між ними. Стрілочка вказує напрям перебігу реакції.
- Число атомів кожного елемента в лівій частині рівняння повинно дорівнювати числу атомів кожного елемента в правій частині рівняння. Для досягнення цього потрібно підібрати і поставити перед формулами відповідні коефіцієнти. Стрілочку в схемі замінити на знак рівності.
?
- Що відбувається з речовинами під час хімічної реакції?
- Що таке хімічна реакція?
- Що відображає схема реакції?
- Яка відмінність між схемою реакції та хімічним рівнянням?
- Де ставлять коефіцієнти у рівнянні реакції?
- Що показують коефіцієнти в рівняннях реакцій?
- Чому складаючи рівняння хімічних реакцій, слід добирати лише коефіцієнти, а індекси міняти не можна?
- Що виражає такий запис: 2Al + 3S = Al2S3?
Узагальнення і систематизація знань з теми «Валентність. Явища. Хімічні рівняння»
Дайте відповіді на запитання
- Як визначити валентність у бінарних сполуках?
- Які фізичні явища можуть супроводжувати хімічні реакції?
- Назвіть умови, необхідні для протікання хімічних реакцій.
- Що ви розумієте під фізичними і хімічними властивостями речовин?
- Наведіть приклади хімічних явищ у побуті.
- Як формулюється закон збереження маси?
- У чому відмінність між схемою реакції і хімічним рівнянням?
- Що відбувається з речовинами під час протікання хімічних реакцій?
- Пригадайте алгоритм складання хімічних рівнянь.
Закінчіть визначення:
- Валентність – це властивість атомів хімічного елемента …
- Відносна молекулярна маса – це фізична величина, що дорівнює …
- Масова частка елемента – це відношення …
- Явище – це …
- Фізичним називається таке явище, під час якого …
- Хімічним називається таке явище, при якому …
- Властивості – це ознаки, за якими …
- Хімічне рівняння – це умовне зображення …
- Вихідними називають речовини, які вступають …
- Продуктами реакцій називають речовини, які …
Виконайте письмово
Тематичне оцінювання 2
| Бал | І варіант | ІІ варіант |
| 0,5 | 1. Які фізичні явища супроводжують хімічні реакції: а) випадання осаду; б) підвищення тиску; в) виділення запаху. |
1. Які фізичні явища супроводжують хімічні реакції: а) зміна забарвлення; б) виділення світла; в) змішування речовин. |
| 0,5 | 2. Якими є умови виникнення і перебігу хімічної реакції: а) приведення в контакт реагуючих речовин; б) розчинення речовин? |
2. Якими є умови виникнення і перебігу хімічної реакції: а) дія світлом; б) перехід твердого стану в рідкий? |
| 1,0 | 3. Чи відбувається хімічне явище при роботі двигуна автомобіля? Чому? | 3. Чи відбувається хімічне явище при куванні металу? Чому? |
| 1,0 | 4. Визначіть масову частку (%) Оксигену у сполуці: N2O5. | 4. Визначіть масову частку (%) Оксигену у сполуці: Fe2O3. |
| 2,0 | 5. Визначіть валентність елементів у сполуках: CH4, PH3, BaO, Al2O3, K2O. |
5. Визначіть валентність елементів у сполуках: Fe2O3, FeO, AgCl, ZnBr2, Cu2O. |
| 2,0 | 6. Складіть формули сполук за валентністю: Na(I)O, CaO, Sn(IV)O, B(III)O, N(V)O, S(VI)O. |
6. Складіть формули сполук за валентністю: K(I)O, ZnO, Fe(III)O, S(IV)O, P(V)O, Cr(VI)O. |
| 2,0 | 7. Складіть формули продуктів реакцій і поставте коефіцієнти в рівняннях реакцій (валентності елементів вказані в дужках): Al + S → Al(III)S(II) P+ O2 → P(V)O |
7. Складіть формули продуктів реакцій і поставте коефіцієнти в рівняннях реакцій (валентності елементів вказані в дужках): Li +O2 → Li(I) O N2+ H2 → N(III)H |
| 3,0 | 8. Напишіть рівняння реакцій за такими схемами: а) Al + O2 → Al2O3; б) Zn + HCl → ZnCl2 + H2; в) Fe(OH)3 → Fe2O3 + H2. На прикладі реакції (а) доведіть розрахунком закон збереження маси. |
8. Напишіть рівняння реакцій за такими схемами: а) Fe + O2 → Fe3O4; б) Al + Br2 → AlBr3; в) Al(OH)3 → Al2O3 + H2. На прикладі реакції (а) доведіть розрахунком закон збереження маси. |



















3 коментарі
Маша
Боже вы меня спасли спасибо вам огромное
Маша
Дякую
Олена
Прекрасно подана інформація. Дуже дякую!!!