Хімічні реакціі
Хімічними реакціями називають явища, при яких одні речовини, що мають певний склад і властивості, перетворюються на інші речовини з іншим складом й іншими властивостями. При цьому в складі атомних ядер змін не відбувається.
Розглянемо типову хімічну реакцію: згоряння природного газу метану (СН4) у кисні повітря.
СН4 + 2О2 = СО2 + 2Н2О
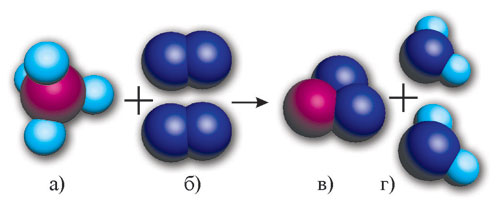
Рис. 51. Горіння метану: а) метан; б) кисень; в) вуглекислий газ; г) вода
Метан і кисень реагують між собою з утворенням вуглекислого газу СО2 і води Н2О. Відбувається перегрупування атомів. На рисунку добре видно, що для успішного здійснення цієї реакції на одну молекулу метану треба дві молекули кисню. Кількість атомів у лівій і правій частинах рівняння однакова. У лівій частині один атом Карбона в складі молекули метану СН4 і в правій той самий атом Карбону ми знаходимо в складі молекули СО2.
Явища, що супроводжують хімічні реакції
Досить часто хімічні реакції можуть супроводжуватися одним або кількома такими зовнішніми ефектами: виділенням чи поглинанням теплоти, утворення нової речовини з виникненням спалаху, появою полум’я, випромінюванням світла, зміною забарвлення речовин, утворенням чи розчиненням осаду, виділенням або зникненням газу, появою, зникненням, чи зміною запаху. Майже в усіх хімічних реакціях У багатьох випадках з цих фізичних ознак можна судити, чи пройшла хімічна реакція чи ні.
Якщо в полум’я пальника внести блискучу магнієву стрічку, вона спалахне і згорить, випромінюючи яскраве світло й велику кількість теплоти. Ознаками цієї реакції є виділення теплоти і світла, зміна кольору, тому що утворюється нова речовина магній оксид MgO у вигляді білого порошку.
Покладемо в пробірку 1-2 гранули цинку і добавимо розчину хлоридної кислоти. Закриємо пробірку корком з газовідвідною трубкою. Спостерігаємо виділення газу.
Зберемо газ у пробірку, надіту на газовідвідну трубку, перевіримо його на чистоту. Для цього піднесемо сірник збоку до нижнього краю пробірки. Чистий газ дає глухий хлопок. Він горить яскравим полум’ям.
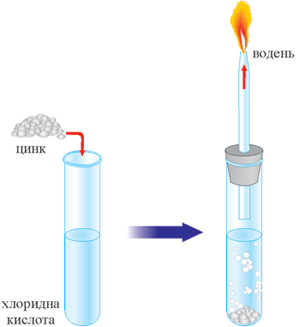
Рис. 52. Взаємодія цинку з хлоридною кислотою.
До незначної кількості амоній хлориду NH4Cl додамо 1-2 мл розчину лугу і злегка нагріємо. Відчуваємо запах амоніаку.
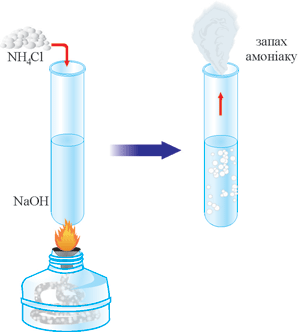
Рис. 53. Взаємодія амоній хлориду з розчином лугу.
Лабораторна робота №2. Дослідження зовнішніх ефектів, що супроводжують хімічні реакції
Дослід 1. Запаліть сірник. У результаті реакції горіння виділяється світло і теплота, сірник обвуглюється. Яке явище відбулося? Чому сірник обвуглився? Який зовнішній ефект реакції горіння?
Дослід 2. Налийте в одну пробірку 1-2 мл розчину ферум(ІІІ) хлориду, а в другу – ферум(ІІ) сульфату і в обидві пробірки добавте по 1-2 мл розчину лугу. Спостерігаємо утворення бурого в першому випадку і зеленувато-білого осаду в другому випадку. Який зовнішній ефект реакції цих реакцій?
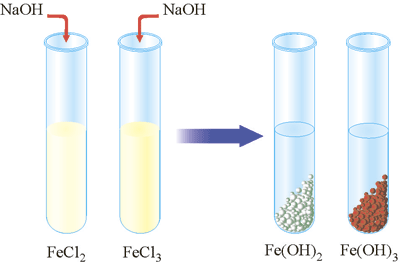
Рис. 54. Взаємодія ферум(ІІІ) хлориду та ферум(ІІ) сульфату з розчином лугу.
Дослід 3. До добутого осаду добавте розчин хлоридної кислоти. Що спостерігаєте?
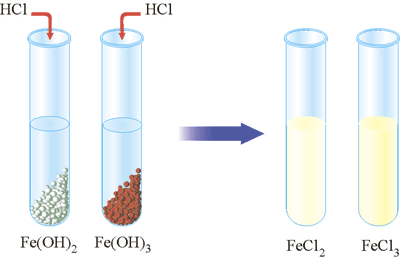
Рис. 55. Взаємодія ферум(ІІІ) гідрокиду та ферум(ІІ) гідрокиду з розчином кислоти.
Але такі ефекти можна спостерігати і під час певних фізичних перетворень.Далеко не завжди за зовнішнім виглядом речовини можна судити про виникнення хімічної реакції. Зовнішньою ознакою саме хімічної реакції може бути виникнення полум’я, але реакції, за яких відбувається горіння речовини, дуже мало.
Щоб дослідити, яке перетворення відбулося – фізичне чи хімічне слід всебічно дослідити властивості речовин до і після реакції і тільки тоді зробити висновок.
Умови хімічних реакцій
Для перебігу переважної більшості хімічних реакцій потрібно створювати певні умови.
Що слід робити, щоб почалася реакція?
Насамперед треба, щоб речовини які реагують, якнайтісніше стикалися одна з одною.
Усім відомо, що поліно важче підпалити, ніж тоненьку скіпочку. Ще важче займається шматок вугілля, а вугільний пил спалахує легко й інтенсивно згоряє. Отож, чим краще подрібнені речовини, то більша у них поверхня стикання і скоріше відбувається реакція між ними. Подрібнення речовин на найменші частинки можна досягти розчиненням деяких з них. Тому попередне розчинення вихідних речовин прискорює взаємодію між ними.
Однією з умов прискорення хімічної реакції є перемішування. Із життевого досвіду вам відомо, що цукор швидше розчиниться у воді, якщо вода буде гарячою, цукор подрібненим, а суміш – перемішуватиметься. Яке явище ми тут спостерігаємо? Фізичне.
У деяких випадках стикання речовин досить, щоб відбулася реакція. Але часто самого тільки стикання речовин для цього не достатньо. Щоб магнієва стрічка горіла, її необхідно нагріти лише до початку реакціі, а далі реакція відбувається самостійно з виділенням тепла і світла. Якщо за допомогою лінзи направити пучок світла на деревину, то через деякий час деревина почне обвуглюватися і може спалахнути. Процес обвуглення триватиме доти, доки сконцентрований пучок світла діятиме на деревину, і припиниться, якщо він зникне. Можна дійти висновку, що на виникнення і перебіг хімічних реакцій нагрівання діє по-різному. Для взаємодії одних речовин потрібне безперервне нагрівання, а для інших – тільки на початку.
Швидкість реакцій між газами зростає з підвищенням тиску.
Схема 2. Зовнішні ефекти хімічних реакцій.
| ЗОВНІШНІ ЕФЕКТИ ← РЕАКЦІЇ → УМОВИ | |||
| 1. Поява світла, зміна температури. |  |
1. Приведення в контакт речовин, що реагують. |  |
| 2. Зміна або зникнення кольору. |  |
2. Подрібнення. |  |
| 3. Утворення осаду. Розчинення осаду. |  |
3. Перемішування. |  |
| 4. Виділення газу. |  |
4. Збільшення тиску (для газів). |  |
| 5. Поява або зникнення запаху. |  |
5. Підігрівання. Дія світла. |  |
Значення хімічних реакцій
З хімічними явищами людина ознайомилася задовго до виникнення науки про них. Відкриття реакції горіння допомогло людині обігрівати житло, готувати їжу, виплавляти метал з руд. Енергія, що виділяється в результаті хімічних реакцій, широко використовується у побуті, на виробництві, під час запуску космічних кораблів та інше. Хімія дає змогу синтезувати невідомі речовини, яких у природі не існує: лікарські препарати, пластмаси, синтетичні барвники, тощо. Хімічні реакціі постійно відбуваються у нашому організмі й забезпечують процеси його життедіяльності. Однак, крім бажаних реакцій, можуть бути реакції небажані: іржавіння заліза, гниття, горіння. Знаючи властивості речовин, такі реакції можна сповільнит або припинити.
Підсумок
- Коли одні речовини перетворюються на інші, відмінні за складом і будовою, це означає, що відбулася хімічна реакція.
- Для того, щоб відбулася хімічна реакція, необхідна одна або кілька названих умов: приведення в контакт реагуючих речовин, подрібнення, перемішування, нагрівання або дія світлом, збільшення тиску для газів.
- Зовнішні ефекти хімічних реакцій: утворення нової речовини з виникненням спалаху, появою полум’я, зміною забарвлення речовин, утворенням чи розчиненням осаду, виділенням або зникненням газу, появою, зникненням, чи зміною запаху.
?
- Які зовнішні ефекти супроводжують хімічні реакції?
- Які умови необхідні для виникнення й перебігу хімічних реакцій?
- Яке значення в практичній діяльності людини має знання умов виникнення й перебігу хімічних реакцій?
- Чому з підвищенням температури хімічні процеси прискорюються?
- Чому проводячи хімічні реакції, здебільшого користуються розчинами.а не твердими речовинами?
Допитливим
• У кожній клітині нашого тіла, а їх у нас 100 трильонів, злагоджено відбувається десятки тисяч хімічних реакцій.
• У пригодницьких романах розповідається про листи, написані безбарвними чорнилами: вороги не знають секретів тайнопису, а хоробрі герої можуть перетворити невидиме у видиме. Уся таємниця полягає в тому, що деякі безбарвні речовини при нагріванні змінюються хімічно і перетворюються у забарвлені. До таких належать сік лимона, цибулі тощо.
Домашній експеримент
Тайнопис
 1. Спробуйте написати соком цибулі або лимона щось на білому листку паперу: нічого не видно. Дайте висохнути малюнку. Малюнок та надпис після висихання непомітні. Проявити їх можна за допомогою гарячої праски, або потримати папір над гарячою плитою, так щоб папір не зайнявся. Колір стає темно-брунатним, написане стає чітко помітним. Яке явище відбулося?
1. Спробуйте написати соком цибулі або лимона щось на білому листку паперу: нічого не видно. Дайте висохнути малюнку. Малюнок та надпис після висихання непомітні. Проявити їх можна за допомогою гарячої праски, або потримати папір над гарячою плитою, так щоб папір не зайнявся. Колір стає темно-брунатним, написане стає чітко помітним. Яке явище відбулося?
2. Запаліть свічку, зверніть увагу на те, чи весь парафін згоряє. Піднесіть у верхню частину полум’я холодний предмет. Про що свідчить утворення копоті на предметі? Які явища відбуваються під час горіння свічки?


















