Усе багатство навколишнього світу викликано тим, що окремі атоми здатні міцно зв’язуватися один з одним і утворювати прості речовини та входити до складу складних речовин. Як із невеликої кількості літер утворюється величезна кількість слів, так із невеликої кількості атомів утворюються мільйони різних речовин. Атоми за звичайних умов не можуть довго існувати поодинці (за винятком елементів інертних газів). Вони сполучаються з такими ж чи іншими атомами й утворюють безліч різноманітних речовин. Усе розмаїття речовин визначається тим, у якому співвідношенні і яким чином атоми поєднуються один з одним.
Хімічні сполуки є комбінацією з двох і більше хімічних елементів.
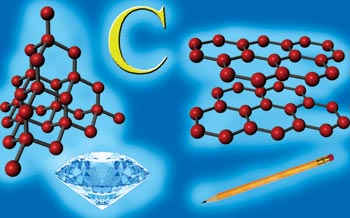
Рис. 42. Прості речовини утворені атомами Карбону: алмаз і графит.

Рис. 43. Прості речовини утворені атомами елемента Ауруму: золота підвіска, ланцюжок, монета, колечко.
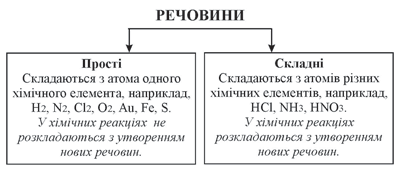
У залежності від того, які елементи входять до складу речовин, речовини поділяють на прості й складні.
Схема 1. Класифікація речовин
Прості речовини
Молекула кисню, необхідного для дихання, складається з двох атомів Оксигену. Формула кисню – О2. Газ водень, формула якого Н2, складається з двох атомів Гідрогену. Золото являє собою набір атомів того самого виду – атомів Ауруму. Золото – проста речовина. Графітові стрижні олівців, вугілля, алмаз (формула яких С) – утворені атомами Карбону.
Прості речовини поділяють на метали і неметали.
До металів належать залізо, цинк, алюміній, золото, мідь, ртуть, срібло, свинець, олово, вольфрам тощо.

Рис. 44. Зразки металів.
Метали як прості речовини, складаються з атомів і мають низку спільних властивостей. Їх атоми міцно сполучені між собою, тому майже всі вони за звичайних умов перебувають у твердому стані. Метали непрозорі, мають характерний «металічний» блиск, добре проводять електричний струм і теплоту, пластичні, ковкі.
Візьмемо для прикладу залізо. Це сріблясто-білий метал, твердий, ковкий, пружний, проводить електричний струм, має металічний блиск, намагнічується. Чимало металів за фізичними властивостями і кольором подібні до заліза. Однак деякі метали можуть мати інший колір. Наприклад, мідь червоного кольору, золото – жовтого. Метал ртуть – рідкий (за звичайних умов), стибій – крихкий.
До неметалів належать фосфор, сірка, графіт, бром, йод, кисень, водень, кремній тощо. Неметалів значно менше, ніж металів.

Рис. 45. Зразки неметалів: червоний фосфор, сірка, вугілля.
Поміркуй! Чому поділ на метали і неметали умовний.
З двох атомів складаються молекули таких простих речовин: Н2, О2, N2, Cl2, Br2, J2, F2.
Поміркуй! Чи можна сказати, що елемент Купрум має металічний блиск?
Частина неметалів складається з атомів, наприклад, алмаз, графіт, червоний фосфор, інертні гази. Більшість неметалів складаються з молекул. Вони не мають такої яскравої зовнішньої схожості, як метали. Неметали не мають «металічного» блиску, погано проводять електричний струм і теплоту, крихкі, м’які, мають різний колір, різний агрегатний стан за нормальних умов, наприклад, водень – безбарвний газ, бром – бура рідина, графіт – тверда чорна речовина.
Візьмемо для прикладу сірку. Це тверда жовта речовина, яка не має металічного блиску, крихка, не проводить електричного струму, погано проводить тепло. Інші неметали подібні за фізичними властивостями до сірки. Однак серед неметалів є й такі, що мають металічний блиск – кремній, йод. Графіт проводить електричний струм. Кремній – напівпровідник, плавиться як і більшість металів, за доволі високої температури (+1420ºС). Серед неметалів є рідини, гази і тверді речовини.
Таким чином, неможливо провести чіткої межі між металами і неметалами. Незважаючи на умовність поділу простих речовин на метали і неметали, його вважають доволі зручним.
Хімічні елементи, від яких походять метали, називають металічними, а ті, що утворюють неметали, неметалічними. Металічних елементів більше, як неметалічних.
Таблиця 4. Назви найпоширеніших простих речовин та відповідних хімічних елементів, що їх утворюють
| Назва простої речовини | Формула простої речовини | Назва відповідного хімічного елемента | Тип |
| Цинк | Zn | Цинк | метал |
| Залізо | Fe | Ферум | метал |
| Алюміній | Al | Алюміній | метал |
| Мідь | Cu | Купрум | метал |
| Магній | Mg | Магній | метал |
| Золото | Au | Аурум | метал |
| Ртуть | Hg | Меркурій | метал |
| Олово | Sn | Станум | метал |
| Свинець | Pb | Плюмбум | метал |
| Срібло | Ag | Аргентум | метал |
| Нікель | Ni | Нікол | метал |
| Водень | H2 | Гідроген | неметал |
| Кисень, Озон | O2, O3 | Оксиген | неметал |
| Сажа, графіт, алмаз | C | Карбон | неметал |
| Сірка | S | Сульфур | неметал |
| Азот | N2 | Нітроген | неметал |
| Фтор | F2 | Флуор | неметал |
| Фосфор (білий, червоний) | P | Фосфор | неметал |
| Йод | I2 | Йод | неметал |
| Бром | Br2 | Бром | неметал |
| Кремній | Si | Силіцій | неметал |
| Хлор | Cl2 | Хлор | неметал |
Назви простих речовин часто збігаються з назвами тих елементів, якими вони утворені. Слід пам’ятати, що назва елемента пишеться з великої літери, а назва простої речовини – з малої. Проста речовина цинк (цинкова пластина, шматочок цинку) складається з атомів елементу Цинку; проста газувата речовина хлор – з атомів елементу Хлору. Інколи назва простої речовини і назва елементів, що утворили цю речовину – різні. Проста речовина мідь (мідна пластинка та ін.) складається з атомів елементу Купруму; кисень – з атомів елементу Оксигену; водень – з атомів елементу Гідрогену, залізо – з атомів елементу Феруму.
Оскільки назви хімічних елементів часто збігаються з назвами простих речовин, потрібно розрізняти поняття «хімічний елемент» і «проста речовина». Не можна приписувати хімічному елементу властивостей, характерних для простої речовини.
Таблиця 5. Порівняння хімічного елемента і простої речовини
| Проста речовина | Хімічний елемент |
| Складається з атомів одного хімічного елемента. | Складова частина речовини – один вид атомів. |
| О2 – кисень, О3 – озон, Cu – метал мідь. | Оксиген – в складі молекули кисню, озону. Купрум – в складі міді. |
Підсумок
- Причиною багатоманітності речовин є здатність атомів сполучатися між собою з утворенням простих і складних речовин.
- Прості речовини складаються з атомів одного хімічного елемента.
- Характерні властивості простих речовин:
| ПРОСТІ РЕЧОВИНИ | |
| Метали (Nа, K, Ca, Ba, Mg, Zn, Al, Fe та інші) | Неметали (S, P, N2, C, O2 та інші) |
| 1. Мають металічний блиск. | 1. Не мають металічного блиску. |
| 2. Електропровідні. | 2. Не електропровідні. |
| 3. Теплопровідні. | 3. Погано проводять тепло. |
| 4. Ковкі, пластичні. | 4. Рідини, гази. Тверді речовини – крихкі, м’які. |
| 5. Мають високу температуру плавлення. | 5. Температури плавлення низькі. |
?
- Чому існує так багато речовин?
- Які речовини називаються простими?
- Назвіть дві групи відомих вам простих речовин.
- За якими ознаками і властивостями можна відрізнити метал від неметалу, чи є чітка відмінність між ними?
- Чого в природі більше: хімічних елементів чи простих речовин; простих чи складних речовин? Чому?
- Скільки видів атомів може входити до складу простої речовини?
- Чим, на вашу думку, метали відрізняються від неметалів?
- Чому речовини поділяють на прості і складні?
Допитливим
• Уже в VIII столітті до нашої ери люди вміли виплавляти і обробляти метали. Розплавленому металові можна надати будь-якої форми. Більшість твердих металів відрізняється міцністю і саме тому з них виготовляють будівельну арматуру, деталі двигунів, де їм доводиться витримувати високі навантаження.

Вироби з металів.
• Метали, навіть найміцніші, інколи ламаються. Руйнування металевих деталей відбувається через постійне навантаження. Це явище називають «втомою металів». Ось чому автомобілі, верстати, літаки регулярно проходять техогляд, який дозволяє виявити ознаки втоми металу і запобігти можливим поломкам.
• Найеластичнішим із металів є золото. З 1 г золота можна витягнути дротину завдовжки до трьох кілометрів, вона у 10 разів тонша за волосину. Золото прокатують у листи завтовшки 8·10–5 мм.

















