Ми вже знаємо, що атоми хімічних елементів зв’язуються між собою, утворюючи прості або складні речовини. Яким чином атоми зв’язуються між собою? Це відбувається тому, що атоми мають таку властивість, як валентність (від латинського слова «valentia», що означає «сила»).
Поміркуй! Скільки зв’язків утворює атом Гідрогену?
Валентність у формулах можна позначити римськими цифрами, які записують над символами хімічних елементів. Валентність має кількісну характеристику. За одиницю прийнято валентність атома Гідрогену. Атом Гідрогену не приєднує більше одного атома інших елементів. Отже, Гідроген одновалентний.
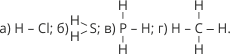
Рис. 46. Графічне зображення хімічних зв’язків у молекулах:
а) HCl; б) H2S; в) PH3; г) CH4.
Розглянемо графічні формули кількох речовин HCl, H2S, PH3, CH4. Із формули HCl видно, що один атом Гідрогену сполучений із одним атомом Хлору. Якщо Гідроген одновалентний, то атом Хлору в HCl теж одновалентний, оскільки він утримує лише один атом Гідрогену. Атом Сульфуру в H2S – двохвалентний, оскільки він утримує два атоми Гідрогену. Відповідно атом Фосфору в сполуці PH3 – тривалентний, а атом Карбону – чотиривалентний. Отже, якщо атом сполучається з двома атомами Гідрогену, то він – двохвалентний, якщо з трьома – тривалентний.
Звідси, валентність елементів, що утворили хімічні зв’язки з Гідрогеном, визначаються числом атомів Гідрогену у формулі.
Проте, Гідроген не утворює сполук із усіма елементами, тому валентність елементів можна визначити за Оксигеном. Оксиген у сполуках двохвалентний.
З періодичної системи елементів Д. І. Менделєєва ми дізнаємося про валентність елементів за Оксигеном. Елементи І групи мають валентність І (за винятком елемента Cu, який проявляє валентність І і в більшості випадків – ІІ); елементи ІІ групи – валентність ІІ, третьої групи – ІІІ. Валентність цих елементів стала. Починаючи з IV групи елементи проявляють змінну валентність. Елементи V групи проявляють валентність V за Оксигеном і три за Гідрогеном; елементи VI групи – шість за Оксигеном і два за Гідрогеном, сьомої групи – сім за Оксигеном і один за Гідрогеном.
У формулах бінарних сполук металічні елементи пишуть на першому місці, а неметалічні – на другому. У такому випадку валентність неметалічних елементів дорівнює 8 мінус номер групи, в якій розміщений цей елемент.
Наприклад: K2S – валентність Калію – І, а Сульфуру – ІІ. (8 – 6 = 2, оскільки Сульфур знаходиться у 6 групі).
Таблиця 8. Валентність атомів деяких елементів у сполуках
| Величина валентності | Металічні елементи | Неметалічні елементи |
| Одновалентні | Na, K, Li, Ag, Cu, Hg | H, Cl, F, Br, I |
| Двовалентні | Mg, Ca, Ba, Zn, Cu, Hg, Fe, Sn, Pb, Cr, Be | O, S, C |
| Тривалентні | Al, Fe, Cr, B | N, Cl |
| Чотиривалентні | Sn, Pb | C, S, Si |
| П’ятивалентні | N, P, Cl | |
| Шестивалентні | Cr | S |
Примітка. Жирним шрифтом виділені елементи зі сталою валентністю.
Дещо складніше визначити валентність за формулами сполук, утворених атомами інших хімічних елементів. Для цього слід пам’ятати такі правила:
- Валентність атомів Гідрогену у сполуках дорівнює одиниці (І), Оксигену – ІІ, Флуору – І.
- Валентність – число ціле – від одного до восьми. Більше восьми або дробовою валентність не існує.
- У бінарних сполуках (складається з двох видів атомів) сумарна валентність усіх атомів одного елемента дорівнює сумарній валентності всіх атомів іншого елемента.
- У назвах речовин, утворених елементом зі змінною валентністю, після назви цього елемента у дужках пишуть римську цифру, яка позначає його валентність. Наприклад: FeO – ферум(ІІ) оксид; Fe2O3 – ферум(ІІІ) оксид.
- У формулах бінарних сполук на першому місці ставлять символи елементів, які у періодичній системі розміщені лівіше або нижче, на другому – які розміщені в періодичній системі правіше або вище: KCl, SO2, OF2. Виняток: NH3, PH3, SiH3.
Визначення валентності елементів за формулами їхніх сполук
Спочатку навчимося визначати валентність елементів за формулами сполук. Якщо формула складається з двох елементів, можна визначити валентність одного елемента, якщо відома валентність іншого.
Приклад: Визначимо валентність Феруму в оксиді Fe2O3.
Валентність Оксигену ІІ, а Феруму – змінна. Щоб визначити валентність Феруму в даній сполуці виконуємо послідовно такі дії:
- Записуємо формулу речовини і над хімічним символом Оксигену позначаємо римською цифрою його валентність:
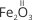
- Валентність Оксигену – два, а таких атомів Оксигену у сполуці є три. Визначаємо сумарну валентність трьох атомів Оксигену: 2 · 3 = 6.
- Ці шість одиниць валентності припадають на два атоми Феруму, тоді на один атом Феруму припадає три одиниці валентності: 6 : 2 = 3. Отже, Ферум в оксиді Fe2O3 – тривалентний.
Визначення валентності
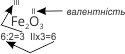
Визначимо валентність елементів у бінарних сполуках за зразком:
1. Пишемо хімічні формули сполук і позначаємо відому валентність елементів: а) ![]() ; б)
; б) ![]() ; в)
; в) ![]() ; г)
; г) ![]() .
.
2. Знаходимо сумарну валентність елемента, валентність якого відома (сумарна валентність позначена під формулою): а) ![]() ; б)
; б) ![]() ; в)
; в) ![]() ; г)
; г) ![]() .
.
3. Сумарну валентність ділимо на число атомів (індекс) елемента валентність якого невідома, і записуємо над хімічним знаком валентність цього елемента: а) 2 : 1 = 2; б) 6 : 1 = 6; в) 2 : 1 = 2; г) 4 : 1 = 4.
4. Відповідь: а) ![]() ; б)
; б) ![]() ; в)
; в) ![]() ; г)
; г) ![]() .
.
Підсумок:
- Валентність – це здатність атомів утримувати один одного в сполуках.
- Зв’язок значення валентності елемента з номером групи періодичної системи:
| Валентність | Номер групи | ||||||
| I | II | III | IV | V | VI | VII | |
| У сполуках з Оксигеном | I | II | III | IV | V | VI | VII |
| У сполуках з Гідрогеном (головних підгруп) | IV | III | II | I | |||
?
- Що таке валентність елементів?
- Назвіть елементи зі сталою валентністю.
- На якому місці у формулах пишуть хімічний знак Оксигену?
- У яких випадках неметалічні елементи пишуть у формулах сполук на першому місці?
- У яких випадках неметалічні елементи пишуть у формулах бінарних сполук на другому місці?
Допитливим
Визначте за структурними схемами валентність кожного елемента, складіть формули цих сполук:
а) O = C = O; б) ![]() ; в)
; в) ![]() .
.



















6 коментарів
Андрій
Я не зрозумів, що це за “гідрогени”, “оксигени” та “сульфури”.
“Водень”, “кисень” та “сірка” вже кимось скасовані?
Ximiya
“Водень”, “кисень” та “сірка” – речовини, а “Гідроген”, “Оксиген” та “Сульфур” – хімічні елементи. Назви хімічних елементів затверджені в Україні за ДСТУ 2439-94, відповідно якого вживаються в науковій літературі.
Наприклад: кисень складається з двох молекул Оксигену, а озон – з трьох.
Докладніше: §7. Хімічні елементи
Тетяна
Вища валентність Нітрогену -ІІІ, в деяких сполуках ІV, а не V. Такої валентності у Нітрогена не буває.
анонім
у Нітрогену вища валентність V
Анна
Цікаво, хто пище про п”ятивалентний Нітроген – діти чи вчителі? Хоча мої восьмикласники, наприклад, вже чудово знають, що п”ятивалентний Нітроген не буває ніколи, оскільки немає можливості переходу у збуджений стан.
світлана
звичайно буває