1. Взаємодія солей з металами
Кожний метал у ряді напруг здатний витісняти всі метали, що стоять справа від нього, з розчинів їх солей з утворенням нової солі та іншого металу. Якщо в пробірку з розчином CuCl2 опустити залізний цвях, то через деякий час він вкриється шаром міді. Відбувається реакція заміщення: CuCl2 + Fe = FeCl2 + Cu.
Схема 8
Хімічні властивості солей
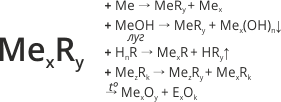
2. Взаємодія солей з лугами
Водні розчини солей можуть взаємодіяти з розчинами лугів, якщо в результаті реакцій одна з новоутворених речовин (сіль, або основа) випадає в осад. Нерозчинні солі з лугами не взаємодіють. Наприклад: ZnCl2 + 2KOH = Zn(OH)2↓ + 2KCl.
3. Взаємодія солей з кислотами
Солі (як розчинні так і нерозчинні) можуть взаємодіяти з кислотами, утворюючи нову кислоту та сіль. Такі реакції часто супроводжуються виділенням газу або осаду, наприклад: NaCl + H2SO4 = Na2SO4 + 2HCl↑.
4. Взаємодія між солями
Реакція між двома солями відбувається лише тоді, коли обидві солі розчинні у воді, а одна з новоутворених солей випадає в осад: ![]() .
.
5. Розкладання солей
Деякі солі під час нагрівання розкладаються. Прикладом таких солей можуть служити карбонати, нітрати, гідрогенкарбонати, сульфіти. Наприклад: 2KNO3 = 2KNO2 + O2; 2NaНCO3 = Na2CO3 + H2О+ CO2.
Лабораторний дослід 8. Взаємодія металів із солями у водному розчині
У пробірку налийте 2-3 мл розчину купрум (II) сульфату і опустіть чистий залізний цвях. Які зміни відбуваються на поверхні металу? Чи змінюється колір розчину? Складіть рівняння реакції.
Лабораторний дослід 9. Взаємодія солей з лугами у водному розчині
У пробірку налийте 2-3 мл розчину купрум (II) сульфату і добавте до нього при перемішуванні кілька крапель розчину натрій гідроксиду. Що спостерігаєте? Яка сполука осаджується?
Лабораторний дослід 10. Реакція обміну між солями в розчині
У пробірку налийте 2-3 мл розчину натрій сульфату і добавте до нього кілька крапель розчину барій хлориду. Що спостерігаєте? Складіть рівняння реакції.


















