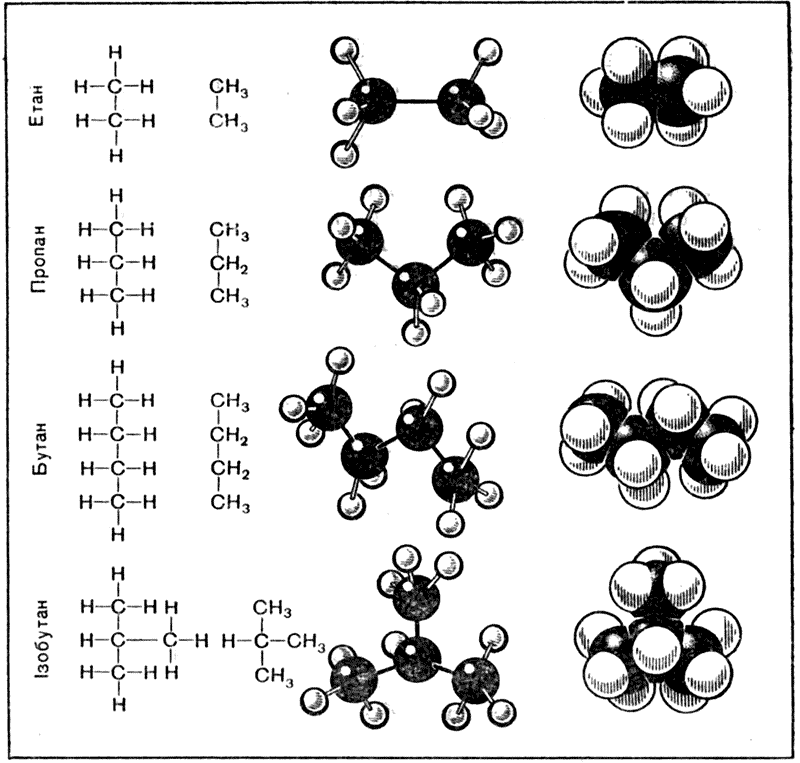
Під час вивчення органічної хімії порівняно з неорганічною значно зростає роль абстракції (гібридизація електронних хмар, просторова ізомерія та інші поняття), збільшується обсяг матеріалу, який не можна підтвердити хімічним експериментом. Виникає необхідність уявляти просторове розміщення молекул. У такому випадку доводиться використовувати моделі. Моделювання – метод експериментального дослідження, який ґрунтується на заміні об’єкта дослідження подібним йому об’єктом (моделлю інших розмірів). Найпростіша кулестержнева модель молекули метану зображена на рисунку 45. Розглянемо просторову будову молекул метану, його гомологів та галогенпохідних (табл. 8).
Таблиця 8. Просторова будова насичених вуглеводнів
|
Молекулярна |
Структурна формула |
Просторова будова гомологів |
Просторова будова ізомерів |
|
СН4 |
|||
|
С2Н6 |
|||
|
С3Н8 |
|||
|
С4Н10 |
Таблиця 9. Моделі молекул метану і його галогенпохідних
|
Сполуки |
СН4 метан |
СН3СI хлор- |
СН2СI2 дихлор- |
СНСI3 трихлор- |
ССI4 тетрахлор- |
|
Моделі молекул |
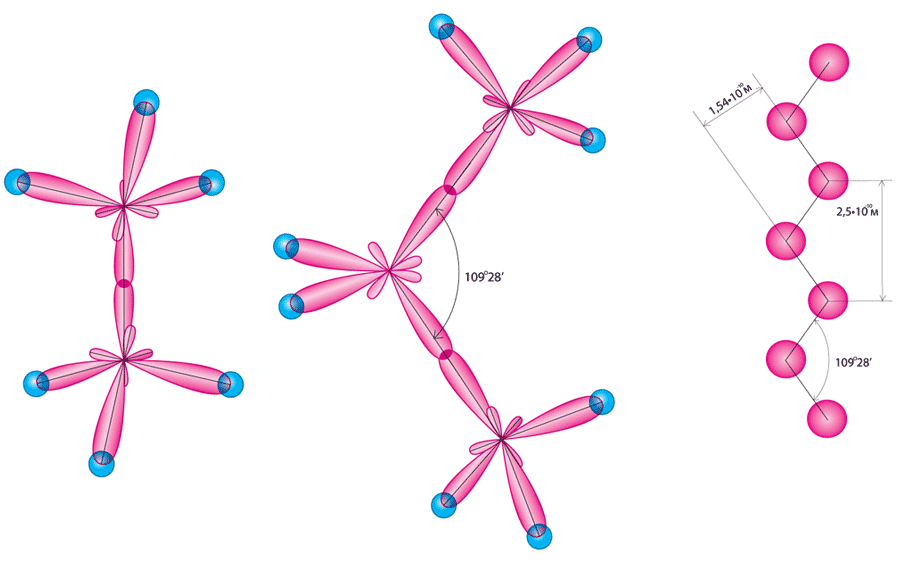
Ми помітили, що молекула метану нагадує тетраедр. У пропані й бутані атоми Карбону розміщені не по прямій лінії, як ми пишемо у формулах, а зигзагоподібно. Причина цього у тетраедричному напрямі валентних зв’язків атомів Карбону. Припустимо, що до атома Карбону приєднався інший атом Карбону. У цього атома залишились ще три вільні валентності, всі вони спрямовані до вершин тетраедра. Другий атом Карбону може приєднатися, очевидно, тільки в одному з цих напрямів. Карбоновий ланцюг у такому разі неминуче набирає зигзагоподібної форми.
Кут між ковалентними зв’язками, які з’єднують атоми Карбону в такому ланцюзі, як й у молекулі метану, 109°28‘. Відстань між сусідніми атомами Карбону, точніше, між центрами атомів становить 1,54А°. Зигзагоподібний ланцюг Карбонових атомів може набувати різних просторових форм. Це зумовлено тим, що атоми в молекулі можуть відносно вільно обертатися навколо хімічних зв’язків.
Подібні моделі добре передають взаємне розташування атомів, направленість зв’язків, але створюють помилкове уявлення про заповнення простору всередині молекули. Використовуючи лише кулестержневі моделі можна помилково прийти до висновку, що органічні молекули нагадують ажурний каркас, також може здаватися, що існує незаповнений простір між атомами, але це не так. В дійсності ніяких «пустих» проміжків в молекулах, як правило, немає, атоми в них щільно прилягають один до одного. Повнішу уяву просторового розміщення молекул дають напівсферичні моделі.
Лабораторний дослід 6. Виготовлення моделей молекул парафінів
Моделі молекул можна зібрати з деталей стандартного заводського ґатунку або виготовити з пластиліну й сірників.
Модель молекули метану. З пластиліну одного кольору виготовте чотири кульки однакового розміру. З пластиліну іншого кольору виготовте кульку, діаметр якої в 1,5 раза більший від діаметра попередніх. На поверхні більшої кульки («атом Карбону») приблизно на однакових відстанях зробіть чотири помітки. В цих місцях вставте стержні (сірники), до кінців яких париєднайте маленькі кульки («атоми Гідрогену»). Ви отримали кулестержневу модель молекули метану.
Виготуйте напівсферичну модель метану. Для цього зробіть на атомі Карбону чотири зрізи під тетраедричними кутами. Зробіть по одному зрізу на чотирьох атомах Гідрогену. Прикладіть зрізами атоми Гідрогену до зрізів атома Карбону.
Модель молекули пропану. З пластиліну одного кольору виготуйте вісім кульок однакового розміру («атоми Гідрогену»). З пластиліну іншого кольору виготуйте три кульки, діаметр яких в 1,5 раза більший від діаметра попередніх. Три кульки більшого діаметра («атоми Карбону») за допомогою сірників (хімічні зв’язки) з’єднайте послідовно між собою під кутом 109°. Відповідно до структурної формули пропану до більших кульок за допомогою стержнів (сірників) приєднайте вісім менших кульок, які умовно зображають атоми Гідрогену.
Модель молекули хлорпропану. З одного стержня моделі молекули пропану зніміть одну маленьку кульку («атом Гідрогену»). Замість неї прикріпіть кульку іншого кольору («атом Хлору»), діаметр якої приблизно в 2 рази більший від діаметра меншої кульки.
Запитання для висновків
- Чому для виготовлення моделей потрібні кульки різних розмірів?
- Яка будова моделі молекули метану?
- Якої форми набув карбоновий ланцюг пропану?
- Як пояснити зигзагоподібну форму карбонового ланцюга?
Підсумок
- Моделі молекул допомагають зрозуміти просторове розміщення органічних сполук.
?
- Які сполуки називаються гомолагами? Наведіть приклади.