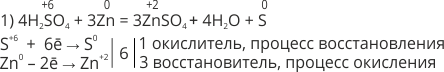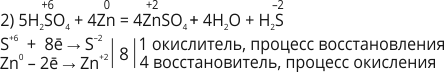Физические свойства
Серная кислота – бесцветная жидкость, тяжелая, почти вдвое тяжелее воды, вязкая как масло. Смешивается с водой в любых соотношениях. При комнатной температуре она нелетучая и поэтому не имеет запаха. При растворении серной кислоты в воде происходит очень сильное разогревание за счет образования устойчивых гидратов серной кислоты. Если вливать воду в кислоту, то часть воды, не успев смешаться с кислотой, сразу нагревается до кипения. Это вызывает разбрызгивание кислоты и может вызвать ожоги.
Концентрированная серная кислота поглощает много влаги. Если открытый стакан с концентрированной кислотой уравновесить на весах, то вскоре чаша со стаканом опустится. Поэтому эту кислоту используют для высушивания веществ. Концентрированная кислота обугливает бумагу и ткань. Попадая на кожу, она вызывает сильные ожоги, поэтому при работе с кислотой необходимо быть очень осторожным. Кислоту, которая попала на кожу или на ткань надо сразу смыть большим количеством воды, затем раствором питьевой соды и снова смыть водой.
Химические свойства
Серная кислота – это сильная кислота. В водном растворе она диссоциирует по схеме: H2SO4 → H+ + HSO4–; HSO4– → H+ + SO42–.
Кислота меняет цвет индикаторов: фиолетовый лакмус становится красным, а метиловый оранжевый – розовым. Разведенная серная кислота имеет общие свойства характерные для всех кислот: она взаимодействует с металлами, основными оксидами, основаниями и солями. Как двухосновная кислота, она образует два рода солей: средние и кислые в зависимости от количественного соотношения реагирующих веществ.
| Кислота | Кислотный остаток | Характер соли |
Общая формула соли, название | Пример |
| H2SO4 | − HSO4 | кислая | Me(HSO4)х гидрогенсульфаты |
KHSO4 – калий гидрогенcульфат Ва(HSO4)2 – барий гидрогенcульфат |
| = SO4 | средняя | Meх(SO4)у сульфаты |
K2SO4 – калий сульфат CaSO4 – кальций сульфат |
Кислые соли — это продукты неполного замещения атомов Гидрогена в молекуле кислоты атомами металлического элемента.
Средние соли — это продукты полного замещения атомов Гидрогена в молекуле кислоты атомами металлического элемента
Химические свойства серной кислоты
1. Взаимодействие с металлами
Разведенная серная кислота взаимодействует с металлами которые в ряду активности стоят до водорода, с выделением водорода и образованием соли. Например: H2SO4 + Zn = ZnSO4 + H2.
2. Взаимодействие с основными оксидами
Серная кислота взаимодействует с основными и амфотерными оксидами с образованием соли и выделением воды, например: CuO + H2SO4 = CuSO4 + H2O
или в ионно-молекулярной форме: CuO + 2H+ = Cu2++ H2O
Этот тип реакций применяют на металлообрабатывающих заводах для очистки поверхности металлических изделий, которые подвергались в процессе изготовления сильному нагреву. Эту операцию называют травлением металла.
3. Взаимодействие с основаниями
Сульфатная кислота взаимодействует с основаниями с образованием соли и выделением воды, например: Cu(OH)2 + H2SO4 = CuSO4 + 2H2O
или в ионно-молекулярной форме: Cu(OH)2 + 2H+ = Cu2+ + 2H2O.
4. Взаимодействие с солями
Как сильная нелетучая кислота, серная кислота вытесняет другие кислоты из сухих солей. Например: H2SO4 + 2KCl → К2SO4 + 2HCl↑.
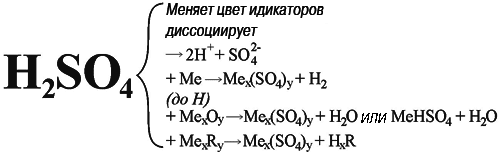
Концентрированная серная кислота
со многими металлами при обычной температуре не взаимодействует. Поэтому безводную кислоту можно хранить в железной таре. Однако при нагревании она взаимодействует почти со всеми металлами (кроме платины и золота). При этих реакциях в зависимости от активности металла может выделяться сера, гидроген сульфид или сульфур(IV) оксид. Реакция происходит по схеме:
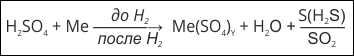 Например:
Например: