Сложных веществ существует в природе и создано человеком больше, чем простых веществ. Вода (Н2О) – сложное вещество, так как состоит из атомов двух видов, его можно разложить на простые вещества – водород (Н2) и кислород (О2). При полном горении простого вещества уголь образуется углекислый газ (СО2), а при неполном горении – угарный газ (СО).
Сложные вещества могут состоять из атомов, молекул или ионов, поэтому их свойства очень многообразны. Атомное строение имеет минерал кварца SiO2 – главная составная часть песка. Он состоит из атомов Оксигена и Силиция. Молекулярным веществом, например, есть вода (Н2О), аммиак (NH3). К ионным соединениям относится много солей, например, поваренная соль (NaCl), негашеная известь (СаО).
Предугадать, какое строение (молекулярное или немолекулярное) имеет данное вещество можно по его физическим свойствам. Вещества с молекулярным строением при обычных условиях – газы (кислород, водород, азот и др.), жидкости (вода, спирт, эфир) или легкоплавкие твердые вещества (серая – температура плавления +113ºС, белый фосфор – температура плавления +44ºС и т.п.).
К веществам с немолекулярным строением относятся соли, кислоты и щелочи.
Таблица 6. Вещества молекулярного и немолекулярного строения
| Признаки для сравнения | Вещества | |
| Молекулярного строения | Немолекулярного строения | |
| Структурные частички вещества | Молекулы | Атомы, ионы |
| Связь между частичками | Слабая | Прочная |
| Температура кипения | Низкая | Высокая |
| Агрегатное состояние (н. у.) | Твердый, редкий, газообразный | Твердый, кристаллический |
| Распространение в природе | Распространены преимущественно в органическом мире | Образуют минералы, горные породы, металлы |
Это объясняется тем, что между молекулами веществ с молекулярным строением химическая связь менее прочна, чем между атомами вещества с атомным строением, поэтому их температуры кипения и плавления сравнительно низкие. У веществ с немолекулярной структурой химическая связь между частицами достаточно прочная, поэтому их температуры плавления и кипения высокие.
Необходимо осознавать разницу между сложными веществами и смесями. Если смешать порошок железа и серы, получим желто-серую смесь, в которой железо и сера сохраняют свои свойства. Новое вещество в результате этого смешивания не образовалось. Если нагреть эту смесь, образуется вещество черного цвета. Она не притягивается магнитом, не разделяется водой на серу и железо. Возникло новое сложное вещество с новыми свойствами. – ферум(II) сульфид (FeS). Этот процесс можно изобразить так:

Сложное вещество от смеси можно отличить по определенным признакам.
Таблица 7. Характерные признаки смесей и химических соединений
| Критерии оценки | Характерные признаки | |
| Смеси | Химические соединения | |
| За составом | Сложное вещество от смеси можно отличить по Вещества можно смешивать в любых массовых соотношениях. | Состав химических соединений постоянный. Пример: молекула воды всегда состоит из одного атома Оксигена и двух атомов Гидрогена. |
| За свойствами | Вещества, входящие в состав смеси, сохраняют свои свойства. | Новое соединение имеет другие свойства относительно веществ, которые образовали данное соединение. |
| За способами разделения | Вещества, входящие в состав смеси, можно разделить физическими способами. | Химические соединения можно разложить только химическими реакциями. |
| За внешними признаками | Механическое смешение не сопровождается признаками реакций. | Образование химических соединений сопровождается признаками химических реакций. |
Лабораторная робота 1. Рассмотрение простых и сложных веществ
Цель: научиться различать простые и сложные вещества.
Вещества: сера, цинк, уголь, железо, пирит, мел, купрум(ІІ) оксид.
На листах бумаги находятся эталоны обычных и сложных веществ с указанными названиями и формулами.
Рассмотрите внешний вид розданных веществ, обратите внимание на этикетки с формулами этих веществ. Определите признак, на основании которого вещества делятся на простые и сложные. Разместите отдельно простые и сложные вещества.
Простые вещества разделите на металлы и неметаллы.
Заполните таблицу:
| Название вещества | Внешний вид | Из каких элементов состоит вещество | Вещество простое или сложное | |
| металл | неметалл | |||
Сделайте вывод:
1. Каков состав простых и сложных веществ?
2. Можно ли по внешнему виду разделить вещества на простые и сложные?
Итог
- Вещества – формы существования химических элементов.
- Если вещество состоит из соединенных между собой атомов разных видов, его называют сложным или химическим соединением.
- Сложные вещества имеют атомное, молекулярное или ионное строение.
?
- На чем основано разделение веществ на простые и сложные?
- Можно ли по внешним признакам разделить вещества на простые и сложные, металлы и неметаллы?
- Из чего состоят простые и сложные вещества?
На досуге
В обведенном столбце зашифрована фамилия ученого, предложившего современную химическую символику.
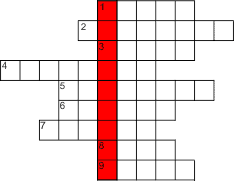
По горизонтали – названия элементов и простых веществ:
1. Элемент, соединение которого используется в медицине в процессе диагностики желудочных заболеваний.
2. Элемент, названный в честь европейской страны.
3. Единый (при обычных условиях) жидкий металл.
4. Изотопы этого элемента загрязняют окружающую среду после того, как произошла авария на ЧАЭС.
5. Название этого элемента происходит от названия материка.
6. Драгоценный металл.
7. Металл, которого выплавляют больше всего на Земле.
8. Название планеты солнечной системы и радиоактивного элемента.
9. Простое вещество, используемое в производстве спичек.

















